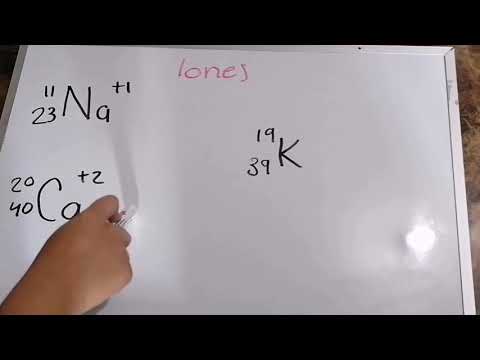En el estudio de la química y la física, es fundamental comprender la estructura de los átomos, las partículas fundamentales que constituyen la materia.
Los átomos están compuestos por electrones, protones y neutrones, y conocer la cantidad de cada una de estas partículas en un átomo es esencial para comprender su comportamiento y propiedades.
En este contenido, exploraremos cómo calcular el número de electrones, protones y neutrones en un átomo, brindando las herramientas necesarias para comprender la estructura atómica y su importancia en el mundo de la ciencia.
Calculando la cantidad de protones, neutrones y electrones
Para calcular la cantidad de protones, neutrones y electrones en un átomo, es necesario conocer su número atómico y su número de masa.
El número atómico (Z) representa la cantidad de protones en el núcleo del átomo, mientras que el número de masa (A) es la suma de protones y neutrones en el núcleo.
1.
Para determinar la cantidad de protones, simplemente se debe mirar el número atómico del átomo.
Por ejemplo, si el número atómico es 6, significa que hay 6 protones en el núcleo.
2.
Para calcular los neutrones, se debe restar el número atómico del número de masa.
Por ejemplo, si el número de masa es 14 y el número atómico es 6, se puede calcular que hay 8 neutrones (14 – 6 = 8).
3.
Por último, para determinar la cantidad de electrones, se debe considerar que los átomos son eléctricamente neutros, lo que significa que tienen la misma cantidad de electrones y protones.
Por lo tanto, si hay 6 protones en el núcleo, también habrá 6 electrones en la nube electrónica que rodea al núcleo.
Es importante destacar que esta regla se aplica a átomos neutros.
En el caso de los iones, que son átomos con carga eléctrica, la cantidad de electrones puede variar.
Por ejemplo, un ion con una carga positiva tendrá menos electrones que protones, mientras que un ion con una carga negativa tendrá más electrones que protones.
Cálculo del número de electrones en un átomo
El cálculo del número de electrones en un átomo se basa en el conocimiento de su configuración electrónica.
La configuración electrónica de un átomo se refiere a la distribución de los electrones en los diferentes niveles de energía o capas electrónicas.
Para determinar el número de electrones en un átomo, se debe seguir el principio de Aufbau, el cual establece que los electrones se distribuyen en los niveles de energía más bajos antes de ocupar los niveles de energía más altos.
Además, se debe seguir el principio de exclusión de Pauli, que indica que cada orbital puede contener como máximo dos electrones con espines opuestos.
La tabla periódica de los elementos químicos es una herramienta útil para determinar la configuración electrónica de un átomo.
Cada elemento tiene un número atómico único, que indica el número de protones en el núcleo del átomo.
Este número también representa el número de electrones en un átomo neutral.
Para determinar la configuración electrónica de un átomo, se puede utilizar el diagrama de orbitales o la notación de configuración electrónica abreviada.
En el diagrama de orbitales, se representan los niveles de energía como cajas y los electrones como flechas.
Cada caja representa un orbital y se llena siguiendo las reglas de Aufbau y Pauli.
Por ejemplo, el átomo de oxígeno tiene un número atómico de 8, lo que significa que tiene 8 electrones.
Su configuración electrónica se puede representar como 1s² 2s² 2p⁴.
Esto indica que el primer nivel de energía (n=1) tiene 2 electrones (1s²), el segundo nivel de energía (n=2) tiene 2 electrones (2s²) y el segundo nivel de energía también tiene 4 electrones (2p⁴).
Número de protones y electrones en los elementos
Los elementos químicos están compuestos por átomos, que a su vez están formados por partículas subatómicas llamadas protones, electrones y neutrones.
El número de protones y electrones en un átomo determinado es esencial para su identificación y clasificación en la tabla periódica.
El número de protones en un átomo se conoce como número atómico y es una de las propiedades más importantes de un elemento.
El número atómico se representa mediante la letra Z y es único para cada elemento.
Por ejemplo, el hidrógeno tiene un número atómico de 1, lo que significa que tiene un protón en su núcleo.
El helio, por otro lado, tiene un número atómico de 2, lo que indica que tiene dos protones en su núcleo.
El número de electrones en un átomo también es igual al número de protones, ya que los átomos son eléctricamente neutros.
Los electrones se encuentran en una nube alrededor del núcleo y están organizados en niveles de energía o capas electrónicas.
El nivel de energía más cercano al núcleo puede contener hasta 2 electrones, mientras que los niveles posteriores pueden contener más.
La configuración electrónica de un átomo nos da información sobre cómo están distribuidos los electrones en sus niveles de energía.
Por ejemplo, el oxígeno tiene una configuración electrónica de 1s2 2s2 2p4, lo que indica que tiene 8 electrones en total: 2 en el primer nivel de energía, 2 en el segundo nivel de energía y 4 en el tercer nivel de energía.
Es importante destacar que el número de protones y electrones en un átomo no siempre es igual al número de neutrones.
Los neutrones son partículas neutras que también se encuentran en el núcleo de un átomo.
El número de neutrones puede variar en un elemento y se representa mediante la letra N.
Por ejemplo, el carbono tiene un número atómico de 6, lo que indica que tiene 6 protones y 6 electrones, pero puede tener diferentes números de neutrones, como el carbono-12 (6 protones y 6 neutrones) o el carbono-14 (6 protones y 8 neutrones).
¡Aprende a contar los componentes atómicos correctamente!