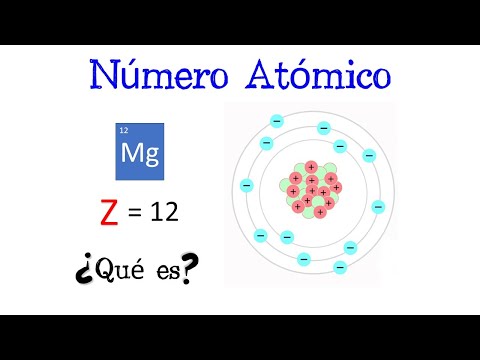
El número atómico de un elemento es una propiedad fundamental que define a cada átomo y determina su lugar en la tabla periódica.
Indica la cantidad de protones en el núcleo de un átomo y, por lo tanto, proporciona información crucial sobre las características y propiedades del elemento.
Además, el número atómico es de gran importancia en química y física, ya que influye en la forma en que los átomos interactúan entre sí y determina su comportamiento químico.
En este contenido, exploraremos en detalle qué indica el número atómico de un elemento y por qué es tan relevante en el estudio de la materia.
Importancia del número atómico en los elementos
El número atómico es un valor fundamental en la tabla periódica de los elementos.
Representa la cantidad de protones que tiene un átomo en su núcleo.
Esta característica es única para cada elemento y no se puede cambiar sin convertir el átomo en otro elemento.
La importancia del número atómico radica en varias razones:
1.
Identificación de los elementos: El número atómico es el principal factor que se utiliza para identificar y clasificar los elementos en la tabla periódica.
Cada elemento tiene un número atómico único, lo que permite diferenciarlos y organizarlos de manera ordenada en la tabla.
2.
Determinación de las propiedades químicas: El número atómico determina las propiedades químicas de un elemento.
La cantidad de protones en el núcleo influye en la distribución de electrones y, por lo tanto, en cómo interactúan los átomos en las reacciones químicas.
3.
Relación con el tamaño del átomo: En general, a medida que aumenta el número atómico, también aumenta el tamaño del átomo.
Esto se debe a que hay más electrones que ocupan niveles de energía cada vez más alejados del núcleo.
Sin embargo, hay excepciones en la tabla periódica debido a la configuración electrónica.
4.
Relación con la carga nuclear efectiva: El número atómico también está relacionado con la carga nuclear efectiva que siente un electrón en un átomo.
A medida que aumenta el número atómico, la carga nuclear efectiva aumenta debido a la atracción electrostática entre los protones y los electrones.
Esto influye en las propiedades físicas y químicas de los elementos.
5.
Relación con la posición en la tabla periódica: El número atómico determina la posición de un elemento en la tabla periódica.
Los elementos están ordenados de manera creciente según su número atómico, lo que permite identificar tendencias y patrones en las propiedades de los elementos a lo largo de las filas y columnas de la tabla.
El número atómico y su significado
El número atómico es una propiedad fundamental de los átomos que se representa con la letra “Z”.
Es un número entero que indica la cantidad de protones que hay en el núcleo de un átomo.
Cada elemento químico tiene un número atómico único que lo distingue de los demás elementos.
El número atómico es una característica determinante de un átomo, ya que define su identidad y sus propiedades químicas.
A medida que el número atómico aumenta, también lo hace la carga positiva del núcleo, lo que a su vez influye en la forma en que los electrones se distribuyen en los niveles de energía.
El número atómico también está relacionado con otras propiedades de un átomo.
Por ejemplo, determina el número de electrones en un átomo en su estado neutro.
Esto se debe a que un átomo neutro tiene una carga total igual a cero, por lo que el número de electrones debe ser igual al número de protones.
Además, el número atómico también se utiliza para organizar los elementos en la tabla periódica.
Los elementos están dispuestos en orden creciente de número atómico, lo que permite identificar patrones y tendencias en las propiedades de los elementos.
Esto facilita el estudio de la química y ayuda a predecir el comportamiento de los elementos y sus compuestos.
Importancia de número de masa y número atómico en identidad de átomo
El número de masa y el número atómico son dos propiedades fundamentales que determinan la identidad de un átomo.
El número de masa (A) es la suma de protones y neutrones en el núcleo de un átomo.
Los protones tienen una carga positiva, mientras que los neutrones no tienen carga.
Por lo tanto, el número de masa es importante porque determina la masa total del átomo.
El número atómico (Z) es igual al número de protones en el núcleo de un átomo.
Los protones tienen una carga positiva, mientras que los electrones tienen una carga negativa y se encuentran en la nube electrónica alrededor del núcleo.
El número atómico es importante porque determina la identidad del elemento químico al que pertenece el átomo.
La combinación del número de masa y el número atómico proporciona información valiosa sobre las propiedades de un átomo.
Por ejemplo, el número de protones determina la carga eléctrica del átomo, mientras que el número de neutrones influye en la estabilidad nuclear.
Además, el número de electrones en un átomo determina su configuración electrónica y, por lo tanto, sus propiedades químicas.
El número de masa y el número atómico también se utilizan para determinar el isótopo de un átomo.
Los isótopos son átomos del mismo elemento que tienen el mismo número atómico pero diferentes números de masa debido a la variación en el número de neutrones.
Estos isótopos pueden tener propiedades físicas y químicas ligeramente diferentes debido a sus masas diferentes.
El número atómico: clave para entender la química.
¡Explora!