En el ámbito de la química y la biología, el estudio de los isómeros ha demostrado ser de vital importancia.
Los isómeros son compuestos que poseen la misma fórmula molecular, pero difieren en su estructura espacial y, por lo tanto, en sus propiedades físicas y químicas.
Esta variación en la estructura molecular puede tener un impacto significativo en cómo los compuestos interactúan en los sistemas biológicos y en los procesos químicos.
En este contenido exploraremos la relevancia de los isómeros en la química y la biología, y cómo su comprensión es fundamental para el avance en estos campos.
Importancia de los isómeros
Los isómeros son moléculas que tienen la misma fórmula molecular, pero difieren en su estructura y, por lo tanto, en sus propiedades físicas y químicas.
Esta propiedad hace que los isómeros sean de gran importancia en varios campos de la química y la biología.
1.
Reactividad química: Los isómeros pueden tener diferentes comportamientos químicos debido a sus diferencias estructurales.
Esto significa que pueden reaccionar de manera diferente con otras sustancias y producir productos diferentes.
Esta capacidad de los isómeros para tener diferentes reactividades químicas es útil en la síntesis de compuestos químicos y en la industria farmacéutica.
2.
Propiedades físicas: Los isómeros pueden tener diferentes puntos de fusión, puntos de ebullición y solubilidades debido a sus diferencias estructurales.
Estas propiedades físicas pueden ser explotadas en la separación y purificación de sustancias químicas.
3.
Identificación y caracterización de compuestos: Los isómeros a menudo tienen diferentes espectros de resonancia magnética nuclear (RMN), espectros de infrarrojos (IR) y espectros de masas.
Esto significa que estos métodos espectroscópicos se pueden utilizar para identificar y caracterizar los isómeros en una mezcla.
Esta capacidad de los isómeros para ser distintos en términos de sus espectros ayuda en la investigación química y en la determinación de la estructura de compuestos desconocidos.
4.
Actividad biológica: Los isómeros pueden tener diferentes efectos biológicos debido a sus diferencias estructurales.
Esto significa que un isómero puede tener propiedades terapéuticas, mientras que otro isómero puede ser tóxico.
Esta propiedad de los isómeros es especialmente importante en la industria farmacéutica, donde la búsqueda de medicamentos efectivos implica la identificación y síntesis de isómeros con la actividad biológica deseada.
5.
Estudio de la estructura y función de biomoléculas: Los isómeros son comunes en las biomoléculas, como los carbohidratos, los lípidos y los aminoácidos.
Estos isómeros pueden tener diferentes funciones biológicas y desempeñar roles importantes en los procesos metabólicos y en la estructura de las células.
El estudio de los isómeros de las biomoléculas es esencial para comprender su estructura y función en los organismos vivos.
Isómeros en biología: una mirada profunda
En el campo de la biología, los isómeros son moléculas que tienen la misma fórmula molecular pero difieren en la forma en la que están dispuestos los átomos.
Esto significa que los isómeros comparten la misma cantidad y tipo de átomos, pero tienen diferentes arreglos espaciales.
Existen diferentes tipos de isómeros en biología, entre ellos se encuentran los isómeros estructurales, los isómeros de posición, los isómeros funcionales y los isómeros estereoisoméricos.
Los isómeros estructurales son aquellos que difieren en la forma en la que están conectados los átomos.
Por ejemplo, el etanol y el metoximetano son isómeros estructurales, ya que ambos tienen la fórmula molecular C2H6O, pero difieren en la forma en la que están dispuestos los átomos de carbono, hidrógeno y oxígeno.
Los isómeros de posición son aquellos que difieren en la posición de un grupo funcional o de una doble enlace.
Un ejemplo de isómeros de posición en biología son el 1-buteno y el 2-buteno, que tienen la misma fórmula molecular C4H8, pero difieren en la posición del doble enlace.
Los isómeros funcionales son aquellos que tienen diferentes grupos funcionales.
Por ejemplo, el propanal y el propanona son isómeros funcionales, ya que ambos tienen la fórmula molecular C3H6O, pero difieren en el grupo funcional.
Mientras que el propanal tiene un grupo aldehído, el propanona tiene un grupo cetona.
Los isómeros estereoisoméricos son aquellos que tienen la misma fórmula molecular y la misma conexión entre los átomos, pero difieren en la orientación espacial de los átomos.
Estos isómeros se dividen en dos categorías: isómeros cis-trans y isómeros enantioméricos.
Los isómeros cis-trans son aquellos que difieren en la orientación espacial de los átomos alrededor de un doble enlace.
Por ejemplo, el ácido maleico y el ácido fumárico son isómeros cis-trans, ya que ambos tienen la fórmula molecular C4H4O4, pero difieren en la orientación de los grupos carboxilo alrededor del doble enlace.
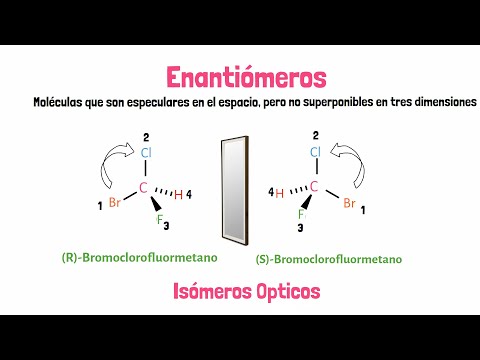
Los isómeros enantioméricos son aquellos que son imágenes especulares no superponibles entre sí.
Esto significa que son moléculas que tienen la misma fórmula molecular y la misma conexión entre los átomos, pero no pueden superponerse.
Un ejemplo de isómeros enantioméricos en biología son los aminoácidos L y D, que son imágenes especulares entre sí.
Isómeros comunes en bioquímica
Los isómeros son compuestos que tienen la misma fórmula molecular, pero difieren en su estructura y, por lo tanto, en sus propiedades químicas.
En bioquímica, existen varios tipos de isómeros comunes que desempeñan un papel crucial en los procesos biológicos.
Algunos de estos isómeros son:
1.
Isómeros estructurales: También conocidos como isómeros de cadena, estos isómeros tienen una fórmula molecular idéntica pero difieren en la forma en que los átomos están unidos entre sí.
Por ejemplo, la glucosa y la fructosa son isómeros estructurales, ya que tienen la misma fórmula molecular (C6H12O6), pero difieren en la organización de sus átomos.
2.
Isómeros geométricos: Estos isómeros se diferencian en la disposición espacial de sus átomos alrededor de un doble enlace.
Un ejemplo común de isomería geométrica en bioquímica es la forma cis-trans de los ácidos grasos insaturados.
En la forma cis, los grupos funcionales están en el mismo lado del doble enlace, mientras que en la forma trans, están en lados opuestos.
3.
Isómeros ópticos: También conocidos como enantiómeros, estos isómeros se diferencian en su capacidad para desviar la luz polarizada.
Tienen la misma fórmula molecular y la misma conectividad de átomos, pero difieren en su configuración espacial.
Los enantiómeros son imágenes especulares no superponibles entre sí.
Un ejemplo famoso de isomería óptica en bioquímica es la forma D y L de los aminoácidos.
4.
Isómeros tautoméricos: Estos isómeros existen en equilibrio químico y pueden interconvertirse rápidamente debido a cambios en la posición de los átomos de hidrógeno.
Un ejemplo importante de isomería tautomérica en bioquímica es la forma cetona y enol de las bases nitrogenadas, como la citosina y la uracilo.
5.
Isómeros conformacionales: Estos isómeros se diferencian en la rotación de los enlaces simples alrededor de un eje de torsión.
No implican cambios en la conectividad de átomos y tienen una energía similar.
Un ejemplo común de isomería conformacional en bioquímica es la forma anti y gauche de los monosacáridos.
Estos son solo algunos ejemplos de los isómeros comunes que se encuentran en bioquímica.
La capacidad de los compuestos para existir en diferentes formas isoméricas es esencial para la diversidad y complejidad de los sistemas biológicos.
No subestimes el poder de los isómeros.