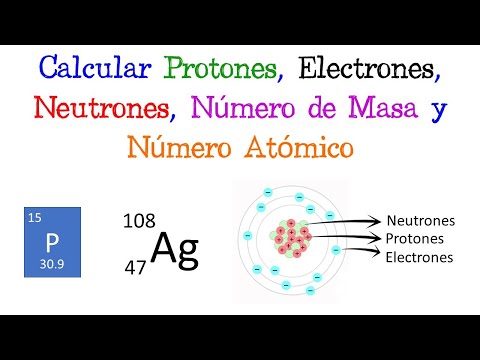
En el estudio de la estructura atómica, es fundamental comprender la composición de los átomos y los diferentes componentes que los conforman.
Uno de estos componentes son los neutrones, partículas subatómicas que se encuentran en el núcleo de un átomo junto con los protones.
El número de neutrones en un átomo puede variar, lo que da lugar a los diferentes isótopos de un elemento.
En este contenido, exploraremos los pasos necesarios para calcular el número de neutrones en un átomo, permitiéndonos obtener una visión más profunda de la estructura atómica y su importancia en la química y otras ramas de la ciencia.
Calculando los neutrones en un átomo
Calcular el número de neutrones en un átomo es una tarea fundamental para comprender su estructura y propiedades.
Los neutrones son partículas subatómicas que se encuentran en el núcleo de un átomo, junto con los protones.
A diferencia de los electrones, los neutrones no tienen carga eléctrica.
Para calcular el número de neutrones en un átomo, se debe conocer la masa atómica del elemento en cuestión.
La masa atómica se expresa en una unidad de medida llamada Unidad de Masa Atómica (uma) o también conocida como Daltons (Da).
Esta unidad representa la masa relativa de un átomo en comparación con la masa de un átomo de carbono-12, que se toma como referencia y se le asigna un valor de 12 uma.
El número de neutrones en un átomo se obtiene restando el número de protones, que es igual al número atómico del elemento, de la masa atómica.
El número atómico se representa con la letra Z y se encuentra en la tabla periódica.
Por lo tanto, la fórmula para calcular los neutrones en un átomo sería:
Número de neutrones = Masa atómica – Número atómico
Por ejemplo, si queremos calcular los neutrones en un átomo de carbono-12, cuya masa atómica es de aproximadamente 12 uma y su número atómico es 6, la fórmula sería:
Número de neutrones = 12 uma – 6 = 6 neutrones
Es importante tener en cuenta que la masa atómica de un elemento puede variar debido a la existencia de isótopos.
Los isótopos son átomos del mismo elemento que tienen diferente número de neutrones.
Por lo tanto, para calcular el número de neutrones en un átomo de un isótopo específico, se debe conocer su masa atómica.
Cálculo de electrones en un átomo
El cálculo de electrones en un átomo es fundamental para comprender su estructura y propiedades.
Los electrones son partículas subatómicas con carga negativa que orbitan alrededor del núcleo del átomo.
El cálculo de electrones se basa en el modelo de capas electrónicas propuesto por Niels Bohr en 1913.
En este modelo, los electrones se distribuyen en diferentes niveles de energía llamados capas.
La capa más cercana al núcleo tiene menor energía y puede contener hasta 2 electrones, mientras que las capas más externas tienen mayor energía y pueden contener más electrones.
Para determinar la distribución electrónica de un átomo, se utiliza el principio de exclusión de Pauli, que establece que dos electrones en un átomo no pueden tener los mismos números cuánticos.
Además, se aplica el principio de máxima multiplicidad de Hund, que dice que los electrones tienden a ocupar orbitales diferentes antes de emparejarse en el mismo orbital.
El número de electrones en un átomo se determina por su número atómico, que corresponde al número de protones en el núcleo del átomo.
Por ejemplo, el átomo de hidrógeno tiene un número atómico de 1, por lo que tiene un solo electrón.
El átomo de carbono tiene un número atómico de 6, por lo que tiene 6 electrones.
La distribución electrónica se representa utilizando el diagrama de configuración electrónica.
En este diagrama, cada capa se representa con una letra (K, L, M, etc.) y se indica el número de electrones en cada capa.
Por ejemplo, el átomo de oxígeno tiene una configuración electrónica de 1s2 2s2 2p4, lo que significa que tiene 2 electrones en la capa 1s, 2 electrones en la capa 2s y 4 electrones en la capa 2p.
El cálculo de electrones en un átomo también es importante para determinar las propiedades químicas y físicas del elemento.
Los electrones en la capa más externa, llamada capa de valencia, son los responsables de las reacciones químicas y la formación de enlaces químicos.
Además, el número de electrones determina la estabilidad del átomo y su tendencia a ganar, perder o compartir electrones para alcanzar una configuración electrónica estable.
Calculando el número atómico
El número atómico es un valor que identifica a cada elemento químico y corresponde a la cantidad de protones que se encuentran en el núcleo de un átomo.
Para calcular el número atómico de un elemento, se deben seguir algunos pasos.
1.
Identificar el símbolo del elemento: cada elemento químico tiene un símbolo único que lo representa.
Por ejemplo, el símbolo del hidrógeno es H y el del oxígeno es O.
2.
Determinar la posición del elemento en la tabla periódica: la tabla periódica es una herramienta importante en química que organiza a los elementos según su número atómico.
Se debe ubicar el elemento en la tabla y recordar su posición.
3.
Contar los protones: el número atómico de un elemento corresponde a la cantidad de protones que tiene en su núcleo.
En la tabla periódica, este valor se encuentra en la esquina superior izquierda del recuadro del elemento.
4.
Anotar el número atómico: una vez contados los protones, se debe anotar este valor como el número atómico del elemento.
Por ejemplo, el número atómico del hidrógeno es 1 y el del oxígeno es 8.
Es importante destacar que el número atómico también determina otras características de un elemento, como su configuración electrónica y su posición en la tabla periódica.
Además, el número atómico puede variar para los isótopos de un mismo elemento, ya que estos difieren en la cantidad de neutrones presentes en el núcleo.
¡Calcula los neutrones en tus átomos ahora!