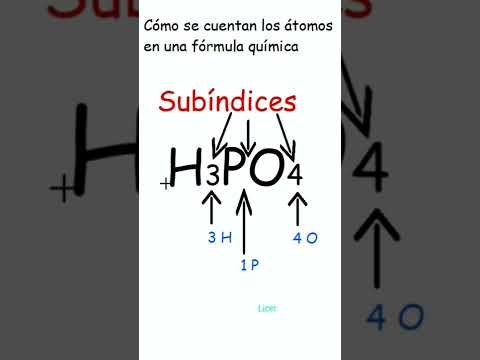
En el fascinante mundo de la química, nos adentramos en un universo donde los átomos son los protagonistas.
Estas diminutas partículas constituyen la base de toda materia y se combinan entre sí para formar compuestos y sustancias nuevas.
Sin embargo, cuando ocurre una reacción química, algo increíble sucede: el número de átomos se modifica.
Es en este proceso donde se desatan cambios asombrosos y se crean nuevas sustancias con propiedades únicas.
En este contenido, exploraremos cómo ocurre esta transformación y cómo afecta a los elementos involucrados.
Prepárate para sumergirte en el emocionante mundo de las reacciones químicas y descubrir cómo los átomos bailan al compás de la química.
¡Bienvenido!
El número de átomos en una reacción química
es una parte fundamental para comprender y balancear las ecuaciones químicas.
Una ecuación química muestra la transformación de los reactivos en productos, y para que esta ecuación esté correctamente balanceada, es necesario que el número de átomos de cada elemento sea igual en ambos lados de la ecuación.
En una reacción química, los reactivos se convierten en productos a través de una serie de reacciones químicas.
Durante estas reacciones, los átomos se reorganizan para formar nuevas sustancias.
Sin embargo, la ley de conservación de la masa establece que la masa total de los reactivos debe ser igual a la masa total de los productos.
Esto implica que el número de átomos también debe ser igual.
Para determinar el número de átomos en una reacción química, es necesario conocer la fórmula química de cada compuesto involucrado.
Cada fórmula química representa la cantidad de átomos de cada elemento presente en el compuesto.
Por ejemplo, la fórmula química del agua (H2O) indica que hay dos átomos de hidrógeno (H) y un átomo de oxígeno (O) en cada molécula de agua.
Una vez que se conocen las fórmulas químicas de los compuestos involucrados, se puede determinar el número de átomos en una reacción química mediante el balanceo de la ecuación química.
El balanceo implica ajustar los coeficientes de los reactivos y productos para que el número de átomos de cada elemento sea igual en ambos lados de la ecuación.
Por ejemplo, consideremos la siguiente ecuación química no balanceada:
CH4 + O2 → CO2 + H2O
Para balancear esta ecuación, se puede comenzar contando el número de átomos de cada elemento en ambos lados de la ecuación.
En el lado izquierdo, hay un átomo de carbono (C) y cuatro átomos de hidrógeno (H).
En el lado derecho, hay un átomo de carbono (C) y dos átomos de oxígeno (O) en el dióxido de carbono (CO2), y dos átomos de hidrógeno (H) y un átomo de oxígeno (O) en el agua (H2O).
Para igualar el número de átomos de carbono, se puede colocar un 1 como coeficiente del CO2.
A continuación, para igualar el número de átomos de hidrógeno, se puede colocar un 2 como coeficiente del H2O.
Finalmente, para igualar el número de átomos de oxígeno, se puede colocar un 2 como coeficiente del O2.
La ecuación química balanceada sería:
CH4 + 2O2 → CO2 + 2H2O
En esta ecuación, se puede ver que hay un átomo de carbono (C), cuatro átomos de hidrógeno (H) y cuatro átomos de oxígeno (O) en ambos lados, cumpliendo con la ley de conservación de la masa y el número de átomos.
Modificaciones en reacción química
Las modificaciones en una reacción química son cambios que ocurren en los compuestos y las moléculas involucradas durante la reacción.
Estas modificaciones pueden ser de diferentes tipos y pueden afectar las propiedades de los compuestos y las moléculas.
1.
Cambios en la estructura molecular: Durante una reacción química, los enlaces entre los átomos en las moléculas pueden romperse y formarse nuevos enlaces.
Esto puede resultar en la formación de nuevas moléculas con una estructura molecular diferente a la de los reactivos iniciales.
Estos cambios en la estructura molecular pueden ser evidentes a través de la observación de propiedades físicas y químicas diferentes en los productos de la reacción.
2.
Cambios en las propiedades físicas: Las modificaciones en una reacción química también pueden manifestarse a través de cambios en las propiedades físicas de los compuestos y las moléculas.
Por ejemplo, una reacción química puede generar un cambio de color, cambio de estado físico (como de sólido a líquido o de líquido a gas), liberación de energía en forma de calor o luz, entre otros.
3.
Cambios en la energía: Durante una reacción química, se puede liberar o absorber energía.
Las modificaciones en la energía pueden ser evidentes a través de cambios en la temperatura de la reacción o en la liberación de calor o luz.
Estos cambios en la energía están relacionados con la formación o ruptura de enlaces químicos en los compuestos y las moléculas involucradas.
4.
Cambios en la cinética de la reacción: Las modificaciones en una reacción química también pueden afectar la velocidad a la que ocurre la reacción.
Esto puede ser evidente a través de cambios en el tiempo necesario para que la reacción alcance su estado de equilibrio o en la velocidad de formación de los productos.
Estos cambios en la cinética de la reacción pueden ser influenciados por factores como la concentración de los reactivos, la temperatura y la presencia de catalizadores.
Cambio en el número de átomos en una reacción
En una reacción química, es común que haya un cambio en el número de átomos debido a la formación y rotura de enlaces químicos.
Este cambio se debe a la conservación de la masa y de la carga en una reacción química.
La ley de la conservación de la masa establece que en una reacción química, la masa total de los reactivos es igual a la masa total de los productos.
Esto significa que el número total de átomos antes y después de la reacción debe ser el mismo.
Para entender cómo cambia el número de átomos en una reacción, es importante conocer la estequiometría de la reacción.
La estequiometría nos dice la proporción en la que los reactivos se combinan para formar los productos.
Esta proporción se expresa a través de coeficientes estequiométricos, que indican el número de moléculas o átomos de cada sustancia involucrada en la reacción.
Cuando se balancea una ecuación química, se ajustan los coeficientes estequiométricos para que el número de átomos de cada elemento sea igual en ambos lados de la ecuación.
Por ejemplo, en la reacción de formación de agua (H2O), se necesitan dos moléculas de hidrógeno (H2) por cada molécula de oxígeno (O2) para formar dos moléculas de agua.
El cambio en el número de átomos también se puede observar al descomponer una sustancia en sus elementos constituyentes.
Por ejemplo, en la reacción de descomposición del agua (H2O), se obtienen dos moléculas de hidrógeno (H2) y una molécula de oxígeno (O2), lo que implica un aumento en el número de átomos de hidrógeno y oxígeno.
En otras reacciones, puede haber una disminución en el número de átomos debido a la formación de compuestos más simples.
Por ejemplo, en la reacción de combustión del metano (CH4), se produce dióxido de carbono (CO2) y agua (H2O), lo que implica una disminución en el número de átomos de carbono e hidrógeno, pero un aumento en el número de átomos de oxígeno.
¡Nunca dejes de explorar el mundo químico!