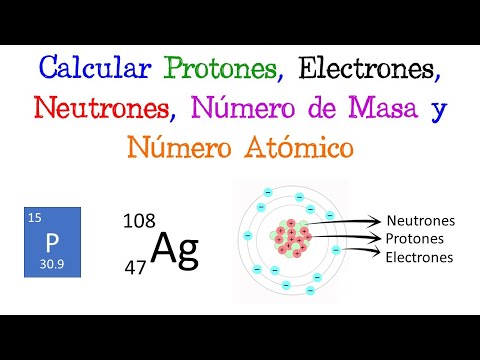
En el mundo de la ciencia y la química, los átomos son los constituyentes básicos de la materia.
Estas diminutas partículas están compuestas por un núcleo central rodeado por electrones en órbita.
Uno de los componentes fundamentales del núcleo es el protón, una partícula cargada positivamente.
En este contenido, exploraremos en detalle el número de protones en el núcleo de un átomo y su importancia en la determinación de las propiedades químicas y físicas de los elementos.
Acompáñanos en este fascinante viaje al mundo subatómico y descubre la fascinante realidad detrás del número de protones en los átomos.
Variación del número de protones en un átomo
El número de protones en un átomo determina su identidad y se conoce como el número atómico.
La variación del número de protones en un átomo puede tener un impacto significativo en sus propiedades químicas y físicas.
1.
Efectos en la carga: Los protones tienen una carga positiva, por lo que un aumento en el número de protones en un átomo resultará en una mayor carga positiva.
Esto influirá en la atracción de los electrones y, por lo tanto, en la estabilidad del átomo.
2.
Cambios en la masa atómica: El número de protones también está relacionado con la masa atómica del átomo.
A medida que aumenta el número de protones, también aumenta la masa del átomo.
Esto se debe a que los protones tienen una masa relativamente grande en comparación con los electrones y los neutrones.
3.
Impacto en la ubicación en la tabla periódica: El número de protones determina el lugar de un átomo en la tabla periódica.
A medida que aumenta el número de protones, el átomo se ubicará en un período más alto y en un grupo diferente.
Esto se debe a que el número de protones determina la configuración electrónica del átomo y, por lo tanto, su comportamiento químico.
4.
Relación con los isótopos: Los isótopos son átomos del mismo elemento que tienen un número diferente de neutrones.
El número de protones en un átomo siempre se mantiene constante para un elemento en particular, pero los isótopos pueden variar en su número de neutrones.
Esto significa que los isótopos tendrán una masa atómica diferente, pero conservarán las mismas propiedades químicas debido al número constante de protones.
Comparación de la cantidad de protones en el núcleo
La comparación de la cantidad de protones en el núcleo de los átomos es fundamental para comprender las propiedades y características de los diferentes elementos químicos.
Los protones son partículas subatómicas con carga positiva que se encuentran en el núcleo de los átomos junto con los neutrones, que son partículas sin carga.
La cantidad de protones en el núcleo de un átomo determina su número atómico, que es una propiedad única de cada elemento químico.
Por ejemplo, el hidrógeno tiene un solo protón en su núcleo, lo que le confiere un número atómico de 1.
Por otro lado, el uranio tiene 92 protones en su núcleo, lo que le da un número atómico de 92.
La comparación de la cantidad de protones en el núcleo de diferentes átomos es esencial para establecer las relaciones periódicas y las tendencias en la tabla periódica de los elementos.
Por ejemplo, los elementos en una misma columna de la tabla periódica, llamados grupos, tienen la misma cantidad de protones en su núcleo.
Esto significa que comparten propiedades químicas similares.
Además, la cantidad de protones en el núcleo también influye en la carga del átomo.
Los electrones, que son partículas con carga negativa, rodean el núcleo y se mantienen en órbitas específicas determinadas por la cantidad de protones.
Si la cantidad de protones es igual a la cantidad de electrones, el átomo es neutro.
Sin embargo, si hay una pérdida o ganancia de electrones, el átomo puede adquirir una carga positiva o negativa, respectivamente.
Núcleo atómico y su carga
El núcleo atómico es el centro del átomo, compuesto por protones y neutrones.
Está rodeado por una nube de electrones que orbitan alrededor de él.
La carga eléctrica del núcleo atómico es positiva debido a la presencia de protones.
Los protones tienen una carga eléctrica positiva de +1.
Por otro lado, los neutrones no tienen carga eléctrica, ya que su carga es neutra (0).
La carga total del núcleo atómico se determina sumando las cargas eléctricas de los protones presentes en él.
Esto se debe a que los electrones, que también tienen carga negativa, se encuentran en regiones alejadas del núcleo y, por lo tanto, su contribución a la carga total del átomo es mínima.
La carga del núcleo atómico es fundamental para determinar las propiedades químicas y físicas de un elemento.
La interacción entre los electrones y el núcleo es lo que permite la formación de enlaces químicos y determina las configuraciones electrónicas de los átomos.
Es importante destacar que la cantidad de protones en el núcleo atómico es lo que define el número atómico de un elemento.
El número atómico es un número entero que representa la cantidad de protones en un átomo.
Por ejemplo, el hidrógeno tiene un número atómico de 1, lo que significa que su núcleo contiene un solo protón.
Recuerda siempre el número de protones.
¡Adiós!